Možnosti použitia inhibítorov DPP4 a SGLT2 u pacientov s diabetes mellitus 2. typu so zníženou funkciou obličiek
Possibilities of using DPP4 inhibitors and SGLT2 inhibitors in patients with type 2 diabetes mellitus with impaired renal function
The incidence and prevalence of diabetes mellitus have grown significantly. Depending on age, duration of diabetes and glycaemic control, a lot of patients with type 2 diabetes will ocur a moderate or severe deterioration of renal function. Moderate renal impairment requieres consideration of dose reduction or treatment cessation for some antidiabetic drugs. All dipeptidyl peptidase inhibitors (DPP4) can be used in mild stages chronic kidney disease, with no need for dose adjustment. However for estimated glomerular filtration (eGF) < 50–60 ml/min/1,73 m2, a dose reduction is required for all DPP-4 inhibitors with exeption of linagliptin. Inhibitors of the renal sodium glucose cotransporter 2 (SGLT2) have been developed to reduce the plasma glucose concentration by inducing glucosuria. Dapagliflozin, canagliflozin and empagliflozin can be safety used in eGF ≥ 60 ml/min/1,73 m2. In patients with eGF < 60 ml/min/1,73 m2, the efficacy decreases and there is an increased incidence of volume/osmotic-related side effects. Dapagliflozin is not recomended in patients who have an eGF < 60/min/1,73 m2. For canagliflozin and empagliflozin, the dose is restricted in patients with an eGF 45–60 ml/min/1,73 m2. When eGF declined to < 45/min. this drugs are contraindicated.
Key words:
type 2 diabetes – DDP4 inhibitors – SGLT2 inhibitor – renal impairment
Autoři:
Vladimír Uličiansky 1; Zbynek Schroner 2
Působiště autorů:
Via medica, s. r. o., Košice
1; SchronerMED, s. r. o., interná a diabetologická ambulancia, Košice
2
Vyšlo v časopise:
Forum Diab 2015; 4(3): 171-176
Kategorie:
Hlavná téma: prehľadová práca
Souhrn
Incidencia a prevalencia diabetes mellitus signifikantne rastie. V závislosti od veku, dĺžky trvania diabetu a glykemickej kompenzácie u veľkého počtu pacientov sa môže vyskytovať mierne až závažné zhoršenie funkcie obličiek. Stredne závažné obličkové poškodenie vyžaduje zváženie zníženia dávky alebo vynechanie niektorých antidiabetických liekov. Všetky inhibítory dipeptidyl peptidázy 4 (DPP4) môžu byť použité pri miernych stupňoch obličkového ochorenia bez úpravy dávky. Pre odhadovanú glomerulovú filtráciu (eGF) < 50–60 ml/min/1,73 m2 je potrebné zníženie dávky všetkých inhibítorov DPP4, s výnimkou linagliptínu. Inhibítory sodíkovo-glukózového kotransportéra 2 (SGLT2) boli vyvinuté na zníženie glykémie v plazme navodením glukosúrie. Dapagliflozín, kanagliflozín a empagliflozín môžu byť bezpečne použité pri eGF ≥ 60 ml//min/1,73 m2. U pacientov s eGF < 60 ml/min/1,73 m2 ich účinnosť klesá a je zvýšená incidencia objemovo-osmotických vedľajších účinkov. Dapagliflozín nie je odporúčaný u pacientov s eGF < 60 ml/min/1,73 m2. Pre kanagliflozín a empagliflozín je znížená dávka u pacientov s eGF 45–60 ml/min/1,73 m2. Pri poklese eGF na < 45/min sú tieto lieky kontraindikované.
Kľúčové slová:
diabetes mellitus 2. typu – inhibítory DPP4 – inhibítory SGLT2 – poškodenie obličiek
Incidencia a prevalencia diabetes mellitus (DM) rastie z celosvetového pohľadu, prevažne v dôsledku vzostupu DM 2. typu (DM2T). Vzostup počtu diabetikov má vplyv na diabetickú nefropatiu (DN – diabetická choroba obličiek), ktorá patrí medzi najčastejšie chronické mikrovaskulárne komplikácie DM [1]. Pre vznik DN je rozhodujúce diabetické prostredie s chronickou hyperglykémiou, ktorá spôsobuje zmeny v štruktúre a funkcii glomerulov, tubulárnych buniek, interstícia ciev v obličkách [2]. U pacienta s DM sa môže vyskytovať celé spektrum obličkových ochorení. Stupeň obličkového poškodenia výrazným spôsobom ovplyvňuje výber antidiabetík v klinickej praxi. Častým limitujúcim faktorom pri výbere farmakoterapie je znížená glomerulová filtrácia (GF). S poklesom GF sa znižuje eliminácia niektorých perorálnych antidiabetík alebo ich aktívnych metabolitov obličkami [3]. Prítomnosť diabetického ochorenia obličiek nielen zhoršuje celkovú a predovšetkým kardiovaskulárnu prognózu diabetikov, ale zvlášť v pokročilých štádiách tiež významne obmedzuje možnosti ich liečby [4]. V závislosti od veku, dĺžky trvania DM a glykemickej kompenzácie u veľkého počtu pacientov môže dôjsť k miernemu alebo závažnému zhoršeniu obličkových funkcií. V ostatných rokoch sa zvýšená pozornosť venuje problematike liečby diabetes mellitus v rôznych stupňoch obličkového poškodenia [5], nielen v kontexte diabetickej nefropatie (DN) alebo aj zo širšieho pohľadu chronického obličkového ochorenia (chronic kidney disease – CKD). Názory sa dynamicky menia pod vplyvom nových poznatkov, ktoré prináša medicína dôkazov, a s uvedením nových antidiabetík do klinickej praxe. Miesto jednotlivých liekových skupín so zohľadnením stupňa poškodenia obličkových funkcií je uvedené v odporúčaniach viacerých medzinárodných odborných spoločností ako sú KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease vypracované National Kidney Foundation – Kidney Disease Improving Global Outcomes [6], ďalej v odporúčaniach Americkej diabetologickej asociácie (ADA) [7,8], Americkej asociácie klinických endokrinológov (AACE/ACE) [9], ale aj v stanovisku Slovenskej nefrologickej spoločnosti a Slovenskej diabetologickej spoločnosti [2].
Medzi modifikovateľné rizikové faktory, ktoré zvyšujú riziko vzniku diabetickej nefropatie, patrí hyperglykémia, fajčenie, artériová hypertenzia, dyslipidémia a vysoký príjem bielkovín. Faktory zvyšujúce riziko progresie diabetickej nefropatie do chronického obličkového zlyhávania sú nasledovné: artériová hypertenzia, proteinúria, fajčenie, nedostatočná kontrola glykémie, dyslipidémia a vysoký príjem bielkovín [2,4]. Vo veľkých prospektívnych randomizovaných štúdiách bolo dokázané, že intenzívna liečba DM s cieľom dosiahnuť skoro normoglykémiu oddialuje začiatok a progresiu zvýšenej exkrécie albumínu v moči a tiež zníženia odhadovanej glomerulovej filtrácie (eGF) u pacientov s DM1T a DM2T [8]. Z klinického pohľadu je dôležité dosiahnuť primeranú glykemickú kompenzáciu včasne po stanovení diagnózy DM, ale klinický význam má aj snaha o metabolickú kontrolu u pacientov s renálnou insuficienciou [5].
Väčšina odborných spoločností odporúča na prevenciu alebo oddialenie mikrovaskulárnych komplikácií DM, vrátane diabetickej nefropatie, cieľové hodnoty HbA1c < 7,0 % DCCT (53 mmol/mol IFCC)[6–8]. Z tohto pohľadu má AACE/ACE prísnejšie kritériá – HbA1c < 6,5 % DCCT (47,5 mmol/mol IFCC), ak tento cieľ nie je limitovaný hypoglykémiou [9]. U pacientov s komorbiditami, zníženou očakávanou dĺžkou života a s rizikom hypoglykémie cieľové hodnoty HbA1c majú byť > 7,0 % DCCT (53 mmol/mol/l IFCC) [6–9].
V závislosti od veku, dĺžky trvania DM a glykemickej kompenzácie, u 20–40 % pacientov s DM2T dochádza k miernemu alebo výraznému zhoršeniu obličkových funkcií. To ovplyvňuje výber antidiabetickej liečby a vyžaduje častejšie monitorovanie obličkových funkcií a glykemickej kompenzácie [5]. Pri výbere antidiabetickej liečby pri obličkovom poškodení je nutné zvážiť metabolizmus a elimináciu lieku, farmakokinetiku a farmakodynamiku pri obličkovom ochorení, glykemickú účinnosť, riziko hypoglykémie, vplyv na telesnú hmotnosť, vplyv na obličkové funkcie a možnosť kombinovanej liečby pri zníženej GF.
Cieľom tejto práce je rozobrať problematiku liečby inhibítormi dipeptidylpeptidázy 4 (DPP4) a inhibítorov sodíkovo-glukózového kotransportéra 2 (SGLT2) pri klesajúcej GF.
Inhibítory dipeptidylpeptidázy 4
Inhibítory dipeptidylpeptidázy 4 (DPP4) predstavujú novú skupinu orálnych antidiabetík. Inhibícia DPP4 zabraňuje degradácii inkretínových hormónov (glukagónu podobného peptidu 1 GLP1 a gastrického inhibičného peptidu GIP), čo vedie k zvýšeniu ich plazmatickej koncentrácie.
Inhibítory DPP4 okrem fyziologickej postprandiálnej stimulácie sekrécie inzulínu vedú k inhibícii postprandiálnej sekrécie glukagónu. Pri ich podávaní dochádza k významnému zníženiu HbA1c, s nízkym rizikom hypoglykémie a bez prírastku na hmotnosti [3,10].
V súčasnosti je na Slovensku dostupných 5 inhibítorov DPP4 – sitagliptín, vildagliptín, saxagliptín, linagliptín a alogliptín. Inhibítory DPP4 po perorálnom podaní majú rôznu absorpciu a distribúciu, rozličné cesty metabolizmu a vylučovania, ale pri zohľadnení špecifík jednotlivých liekov sa všetky môžu používať pri rôznych štádiách chronického obličkového ochorenia [5–13]. U liekov s úpravu dávkovania podľa eGF sa pred začiatkom podávania a pravidelne potom odporúča pravidelné kontrolovanie obličkových funkcií.
Sitagliptín v terapeutických dávkach spôsobuje inhibíciu DPP4, ktorá pretrváva 24 hodín.
Vylučuje sa v 87 % močom (aktívnou tubulárnou sekréciou) a v 13 % stolicou.
Vildagliptín je selektívny a reverzibilný inhibítor DPP4, ktorý zvyšuje endogénnu hladinu inkretínov – GLP1 a GIP. Vildagliptín je v prevažnej miere metabolizovaný v obličkách na inaktívne metabolity, ktoré sú vylučované močom. Približne 85 % dávky vildagliptínu sa vylučuje močom a 15 % dávky stolicou.
Saxagliptín je vysoko účinný, selektívny, reverzibilný, kompetitívny inhibítor DPP4. Saxagliptín je metabolizovaný prevažne v pečeni na aktívne metabolity. Saxagliptín aj jeho aktívny metabolit sú vylučované renálnou a hepatálnou cestou (hlavná je exkrécia obličkami).
Linagliptín je selektívny perorálny inhibítor DPP4. Primárne je vylučovaný žlčou a stolicou, obličková exkrécia je 5 %. V eliminácii linagliptínu hrá metabolizmus menej dôležitú úlohu.
Alogliptín je vysoko selektívny inhibítor DPP4. Nepodlieha rozsiahlemu metabolizmu. Má nevýznamne aktívne metabolity: < 1 % z pôvodného lieku. Močom sa vylúči 60–70 % dávky v nezmenenej forme [5,10,11].
Prehľad dávkovania inhibítorov DPP4 v rôznych štádiách chronickej choroby obličiek (CKD) klasifikovanej podľa KDIGO 2012 je v tab. 1.
![Dávkovanie inhibítorov DPP4 (mg/die) v rôznych štádiách chronickej choroby obličiek (CKD) klasifikovanej podľa KDIGO 2012. Upravené podľa [10]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/367f88f914a2bfe2ec5388289ace6690.png)
Klinické štúdie s inhibítormi DPP4 u pacientov so zníženými obličkovými funkciami
Účinnosť inhibítorov DPP4 u pacientov so zníženými obličkových funkciami bola sledovaná vo viacerých klinických štúdiách s konzistentnými výsledkami [11]. V prospektívnych kontrolovaných štúdiách s dĺžkou trvania viac ako 3 mesiace došlo k zníženiu HbA1c o 0,4 až 1,1 % (DCCT), to je o 4–12 mmol/mol (IFCC) v závislosti od lieku. Pri všetkých inhibítoroch DPP4 bola dokázaná superiorita voči placebu.
Chan et al v 54-týždňovej dvojito zaslepenej randomizovanej štúdii s 91 pacientmi s DM2T so stredne až výrazne zníženou GF (≥ 30 do < 50 ml/min) alebo výrazne zníženou GF (< 30 ml/min), včítane pacientov v terminálnom obličkovom zlyhaní na dialýze sledovali bezpečnosť a účinnosť sitagliptínu v porovnaní s placebom (12 týždňov) a následne glipizidom (42 týždňov). Sitagliptín v dávke 50 mg, resp. 25 mg podľa obličkových funkcií bol dobre tolerovaný s nízkym výskytom hypoglykémií a viedol k poklesu HbA1c o 0,7 % DCCT [14].
Ito et al v prospektívnej otvorenej štúdii u 51 pacientov s DM2T liečených hemodialýzou podávali vildagliptín v dávke 50–100 mg/denne. Priemerná denná dávka bola 80 ± 5 mg. Po 24 týždňoch došlo k poklesu HbA1c z 6,7 % na 6,1 % DCCT a k poklesu postprandiálnej glykémie z 10,3 na 7,8 mmol/l (p < 0,0001). U žiadneho pacienta sa nevyskytli závažné nežiaduce účinky (NÚ)[15].
Lukashevich et al vykonali multicentrickú, randomizovanú, dvojito zaslepenú, placebom kontrolovanú klinickú štúdiu trvajúcu 24 týždňov na stanovenie bezpečnosti a účinnosti vildagliptínu 50 mg 1-krát denne v porovnaní s placebom u 515 pacientov s DM2T so stredne ťažkou poruchou (N = 294) alebo ťažkou poruchou funkcie obličiek (N = 221). Na začiatku klinického skúšania bolo 68,8 % pacientov so stredne ťažkou a 80,5 % s ťažkou poruchou funkcie obličiek liečených inzulínom (priemerná denná dávka bola 56 jednotiek, resp. 51,6 jednotiek). U pacientov so stredne ťažkou poruchou funkcie obličiek liečba vildagliptínom viedla k poklesu HbA1c o 0,5 ± 0,1 % DCCT (p < 0,0001) z východiskovej hodnoty 7,9 %. V skupine s ťažkou poruchou funkcie obličiek došlo k poklesu HbA1c o 0,6 ± 0,1 % DCCT (východisková hodnota 7,7%; p < 0,0001). Bezpečnostný profil vildagliptínu bol podobný ako u placeba [16].
Nowicki et al v randomizovanej dvojito zaslepenej placebom kontrolovanej štúdii v dĺžke trvania 12 týždňov u 170 pacientov dokázali, že saxagliptín v dávke 2,5 mg denne je dobre tolerovanou liečebnou možnosťou u pacientov s nedostatočne kontrolovaným DM2T a s postihnutím obličiek (klírens kreatinínu < 50 ml/min) [17].
McGill et al podávali 133 pacientom s DM2T a s eGF < 30 ml/min/1,73 m2 po dobu 1 roka linagliptín v dávke 5 mg alebo placebo. Rozdiel v poklese HbA1c pri liečbe linagliptínom v porovnaní s placebom bol 0,72 % DCCT (p < 0,0001). Pri liečbe linagliptínom došlo k zníženiu dávky inzulínu o 6,2 jednotiek, pri placebe o 0,3 jednotky. V priebehu štúdie bol nízky výskyt závažnej hypoglykémie, telesná hmotnosť a renálne funkcie boli stabilné [18].
Sakai et al v 6 mesačnej štúdií u 36 pacientov s chronickou obličkovou chorobou zistili, že alogliptín môže byť bezpečne podávaný u pacientov s CKD [19].
Ferreira et al porovnávali sitagliptín a glipizid u 426 pacientov s DM2T s miernym až závažným obličkovým postihnutím po dobu 54 týždňov. Sitagliptín aj glipizid boli rovnako účinné pri znižovaní HbA1c. Sitagliptín bol dobre tolerovaný, s nízkym výskytom hypoglykémie. Liečba sitagliptínom viedla k poklesu hmotnosti v porovnaní s prírastkom hmotnosti pri glipizide [20].
Kothny et al porovnávali vildagliptín a sitagliptín u pacientov s DM2T s ťažkým obličkovým poškodením (eGF < 30 ml/min). V odporúčaných dávkach vzhľadom na obličkovú funkciu vildagliptín (50 mg 1-krát denne) a sitagliptín (25 mg 1-krát denne) mali podobnú účinnosť a boli dobre tolerované [21].
Inhibítory sodíkovo-glukózového kotransportéra 2
K najnovším terapeutickým trendom patria inhibítory sodíkovo-glukózového kotransportéra 2 (SGLT2). Inhibítory SGLT2 (gliflozíny) pôsobia v proximálnom tubule obličiek – znižujú reabsorpciu glukózy, zvyšujú glukosúriu s následným znížením glykémie. Na klinické použitie sú aktuálne dostupné dapagliflozín, kanagliflozín a empagliflozín. Podľa výsledkov klinických štúdií liečba týmito preparátmi vedie k poklesu HbA1c, telesnej hmotnosti a systolického krvného tlaku. Výhodou je nízke riziko hypoglykémie. Najčastejším nežiaducim účinkom sú infekcie urogenitálneho traktu [22–25]. U pacientov s eGF < 60 ml/min/1,73 m2 ich účinnosť klesá a je zvýšená incidencia objemovo-osmotických vedľajších účinkov [26]. V posledných mesiacoch sa diskutuje otázka euglykemickej diabetickej ketoacidózy [27]. V štúdii EMPA-REG OUTCOME pacienti s DM2T s vysokým kardiovaskulárnym rizikom liečení empagliflozínom v porovnaní s placebom mali nižší výskyt primárneho združeného ukazovateľa (kardiovaskulárna mortalita, nefatálny infarkt myokardu a nefatálna cievna mozgová príhoda) a úmrtia z akejkoľvek príčiny po pridaní študovaného lieku ku štandardnej liečbe [28].
Dapagliflozín je vysoko selektívny inhibítor SGLT2. Je metabolizovaný v pečeni a vylučovaný je prevažne renálnou cestou (75 % je exkrécia obličkami). U pacientov s miernym a závažným poškodením funkcie obličiek (klírens kreatinínu < 60 ml/min) sa jeho podávanie neodporúča.
Kanagliflozín je účinný inhibítor SGLT2. Jeho metabolizácia prebieha hlavne v pečeni. Vylučovaný je močom (približne 33 %) a stolicou. U pacientov s klírensom kreatinínu < 60 ml/min sa nemá začať s liečbou kanagliflozínom. U pacientov tolerujúcich kanagliflozín, u ktorých GF klesne trvalo pod 60 ml/min, treba dávku upraviť na 100 mg 1-krát denne. Liečba kanagliflozínom sa má ukončiť, ak je GF trvalo pod 45 ml/min.
Empagliflozín je reverzibilný, účinný, selektívny inhibítor SGLT2. Primárnou cestou metabolizmu empagliflozínu v pečeni je glukuronidácia, nedochádza k vzniku žiadneho aktívneho metabolitu. Vylučovaný je 54,4 % močom (z toho 28,6 % nezmenene ) a 41,2 % stolicou. Empagliflozín sa nemá začať podávať pacientom s eGF < 60 ml/min/1,73 m2. U pacientov, ktorí znášajú empagliflozín a u ktorých eGF trvalo klesá pod 60 ml/min/1,73 m2, sa má dávka empagliflozínu upraviť na 10 mg 1-krát denne alebo sa má dávka 10 mg 1-krát denne udržiavať. Empagliflozín sa má vysadiť, ak eGF trvalo klesne pod 45 ml/min/1,73 m2 [22–26].
Prehľad dávkovania inhibítorov SGLT2 v rôznych štádiách chronickej choroby obličiek (CKD) klasifikovanej podľa KDIGO 2012 uvádza tab. 2.
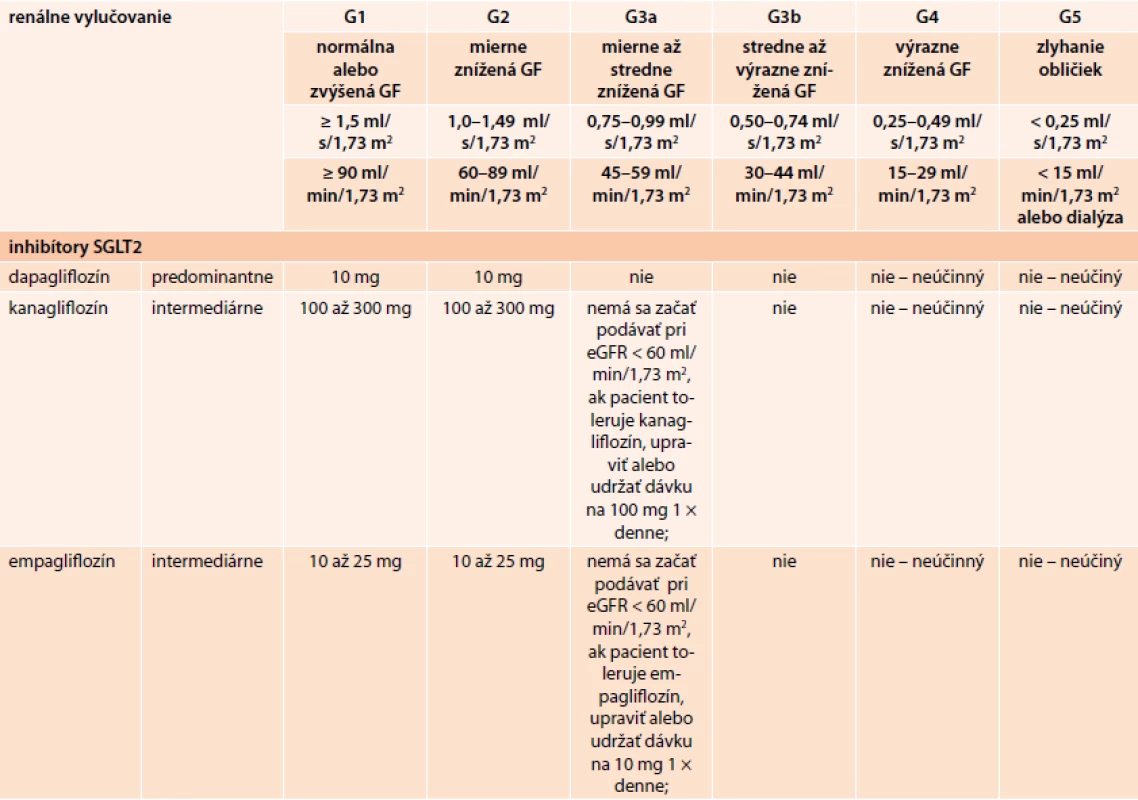
Klinické štúdie s inhibítormi SGLT2 u pacientov so zníženými obličkovými funkciami
Kohan et al podávali v randomizovanej dvojito zaslepenej placebom kontrolovanej štúdii 252 pacientom s DM2T so stredným obličkovým postihnutím dapagliflozín v dávke 5 mg a 10 mg. Po 104 týždňoch nedošlo k štatisticky významnému poklesu HbA1c v porovnaní s placebom. Bol však pozorovaný pokles telesnej hmotnosti a krvného tlaku vs placebo. Po prvom týždni liečby došlo k miernemu vzostupu kreatinínu v sére – dapagliflozín 5 mg o 11,49 mmol/l, dapagliflozín 10 mg o 15,91 mmol/l. Tieto hodnoty sa ďalej nezmenili v priebehu celej štúdie. Priemerné hodnoty elektrolytov sa nezmenili v žiadnej skupine. V porovnaní s placebom bol pri liečbe dapagliflozínom nižší výskyt hyperkaliémie [28].
Yale et al sledovali účinnosť a bezpečnosť kanagliflozínu u pacientov s DM2T v 3. štádiu CKD s eGF ≥ 30 a < 50 ml/min/1,73 m2. V 52 týždňovej randomizovanej dvojito zaslepenej placebom kontrolovanej štúdii sledovali 269 pacientov. Pacienti boli liečení kanagliflozínom v dávke 100 alebo 300 mg a placebom 1-krát denne. Na konci štúdie došlo k zníženiu HbA1c v porovnaní s placebom o 0,27 % (kanagliflozín 100 mg) a 0,41 % (kanagliflozín 300 mg). Pri liečbe oboma dávkami kanagliflozínu došlo k zníženiu glykémie nalačno, telesnej hmotnosti a krvného tlaku. Osmotická diuréza bola častejšia pri liečbe kanagliflozínom. Incidencia urogenitálnych infekcií a deplécia objemu bola vyššia pri kanagliflozíne v dávke 300 mg. V štúdii bol pozorovaný pokles eGF: pri kanagliflozíne v dávke 100 mg o 2,1 ml/min, pri kanagliflozíne v dávke 300 mg o 4,0 ml/min a pri placebe o 1,6 ml/min. Vzhľadom na to, že určitý pokles eGF bol pozorovaný aj u pacientov, ktorí dostávali placebo, usudzuje sa, že tieto zmeny môžu byť skôr vo vzťahu k diabetickej nefropatii ako ku farmakoterapii. Liečba kanagliflozínom viedla k zníženiu pomeru albumín/kreatinín v porovnaní s placebom (-16,4 %, -28 % a 19,7 %) [29].
Barnet et al v štúdii EMPA-REG RENAL zisťovali účinnosť a bezpečnosť empagliflozínu u pacientov s poškodením funkcie obličiek. Štúdia trvala 52 týždňov a zaradených bolo 290 pacientov s eGF ≥ 60 až < 90 ml/min/1,73 m²: placebo (n = 95), empagliflozín 10 mg (n = 98), empagliflozín 25 mg (n = 97) a 374 pacientov s eGF ≥ 30 až < 60 ml/min/1,73 m²: placebo (n = 187), empagliflozín 25 mg (n = 187). Autori zistili, že liečba empagliflozínom je účinná aj u pacientov s poškodením funkcie obličiek [30].

Záver
Inhibítory DPP4 a inhibítory SGLT2 významným spôsobom rozširujú paletu terapeutických možností DM2T. Ich racionálna indikácia vyžaduje rešpektovanie obličkových funkcií. Prehľad použitia inhibítorov DPP4 a inhibítorov SGLT2 pri obličkovom poškodení znázorňuje tab. 3 [5–13,24,25].
V klinickej praxi je dôležité nielen identifikovať problém výberu optimálnej liečby, ale zároveň aj starostlivo monitorovať glykemickú kompenzáciu a obličkové funkcie.
MUDr. Vladimír Uličiansky
vladouli@centrum.sk
Via medica, s.r.o.
www.diaslovakia.sk
Doručené do redakcie 27. 9. 2015
Prijaté po recenzii 13. 10. 2015
Zdroje
1. Tuttle K, Bakrin GL, Bilous RW et al. Diabetic Kidney Disease: A Report From an ADA Consensus Conference. Diabetes Care 2014; 37(10): 2864–2883.
2. Okša A, Ponťuch P, Spustová V et al. Diabetická nefropatia: Diagnostika, prevencia a liečba. Odporúčané postupy Slovenskej nefrologickej spoločnosti a Slovenskej diabetologickej spoločnosti. Forum Diab 2013; 2(2-Suppl 1): 1–6.
3. Uličiansky V, Schroner V, Némethyová Z et al. Personalizovaná medicína v diabetológii v kontexte odporúčaní ADA/EASD 2015. Forum Diab 2015; 4(2): 102–118.
4. Haluzík M. Léčba diabetiků s chronickým onemocněním ledvin. In: Haluzík M, Rychlík I et al. Léčba diabetu u pacientů s onemocněním ledvin a jater. Mladá fronta: Praha 2012 : 63–99. ISBN 978–80–204–2671–0.
5. Bailey CJ, Day C. Diabetes Therapies in Renal Impairment. Br J Diabetes Vasc Dis 2012; 12(4): 167–171.
6. KDIGO 2012. Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int Suppl 2013; 3(1): 1–163. Dostupné z WWW: <http://www.kdigo.org/clinical_practice_guidelines/pdf/CKD/KDIGO_2012_CKD_GL.pdf>.
7. Inzuchi SE, Bergenstal RM, Buse JB et al. Management of hyperglycemia in type 2 diabetes, 2015: Update to a position statement of the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care 2015; 38(1): 140–149.
8. American Diabetes Association Standards of Medical Care in Diabetes – 2015. Diabetes Care 2015; 38(Suppl 1): S1-S93.
9. AACE/ACE Diabetes Guidelines. American Association of Clinical Endocrinologists and American College of Endocrinology – Clinical Practice Guidelines for Developing A Diabetes Mellitus Comprehensive Care Plan – 2015. Endocr Pract 2015; 21(Suppl 1). Dostupné z www: https://www.aace.com/files/dm-guidelines-ccp.pdf.
10. Russo, E, Penno G, Del Prato S. Managing diabetic patients with moderate or severe renal impairment using DPP-4 inhibitors: focus on vildagliptin. Diabetes Metab Syndr Obes: Targets and Therapy 2013; 6 : 161–170.
11. Davis TM. Dipeptidyl peptidase-4 inhibitors: pharmacokinetics, efficacy, tolerability and safety in renal impairment. Diabetes Obes Metab 2014; 16(10): 891–899.
12. Cheng D, Fei Y, Liu Y et al. Efficacy and Safety of Dipeptidyl Peptidase-4 Inhibitors in Type 2 Diabetes Mellitus Patients with Moderate to Severe Renal Impairment: A Systematic Review and Meta-Analysis. Plos One 2014; 9(10): e111543. Dostupné z DOI: <http://dx.doi.org/10.1371/journal.pone.0111543>.
13. Schroner Z, Uličiansky V. Inhibítory dipeptidyl peptidázy-4 – základná charakteristika a mechanizmus účinku. In: Schroner Z, Uličiansky V. Liečba založená na účinku inkretínov. 2nd ed. SchronerMED: Košice 2011 : 41–61. ISBN 978–80–970714–7-9.
14. Chan JCN, Scott R, Ferreira JCA et al. Safety and efficacy of sitagliptin in patients with type 2 diabetes and chronic renal insufficiency. Diabetes Obes Metab 2008; 10(7): 545–555.
15. Ito M1, Abe M, Okada K et al. The dipeptidyl peptidase-4 (DPP-4) inhibitor vildagliptin improves glycemic control in type 2 diabetic patients undergoing hemodialysis. Endocr J 2011; 58(11): 979–987.
16. Lukashevich V, Schweizer A, Shao Q et al. Safety and efficacy of vildagliptin versus placebo in patients with type 2 diabetes and moderate or severe renal impairment: a prospective 24-week randomized placebo-controlled trial. Diabetes Obes Metab 2011; 13(10): 947–954.
17. Nowicki M, Rychlik I, Haller H et al. Saxagliptin improves glycaemic control and is well tolerated in patients with type 2 diabetes mellitus and renal impairment. Diabetes Obes Metab 2011; 13(6): 523–532.
18. McGill JB, Sloan L, Newman J et al. Long-term efficacy and safety of linagliptin in patients with type 2 diabetes and severe renal impairment: a 1-year, randomized, double-blind, placebo-controlled study. Diabetes Care 2013; 36(2): 237–244.
19. Sakai Y, Suzuki A, Mugihima K et al. Effects of Alogliptin in Chronic Kidney Disease Patient with Type 2 Diabetes. Intern Med 2014; 53(3): 195–203.
20. Ferreira AJC, Marre M, Barzilai N et al. Efficacy and safety of sitagliptin versus glipizide in patients with type 2 diabetes and moderate-to-severe chronic renal insufficiency. Diabetes Care 2013; 36(5): 1067–1073.
21. Kothny W, Lukashevich V., Foley JE et al. Comparison of vildagliptin and sitagliptin in patients with type 2 diabetes and severe renal impairment: a randomised clinical trial. Diabetologia 2015; 58(9): 2020–2026.
22. Bays H. Sodium Glucose Co-transporter Type 2 (SGLP2) Inhibitors: Targeting the Kidney to Improve Glycemic Control in Diabetes Mellitus. Diabetes Ther 2013; 4(2): 195–220.
23. DeFronzo RA, Davidson JA, Del Prato S. The role of the kidneys in glucose homeostasis: a new path towards normalizing glycaemia. Diabetes Obes Metab 2012; 14(1): 5–14.
24. Hasan FM, Alsahli M, Gerich JE. SGLT2 inhibitors in the treatment of type2 diabetes. Diabetes Res Clin Pract 2014; 104(3): 297–322. Dostupné z DOI: <http://dx.doi.org/10.1016/j.diabres.2014.02.014>.
25. Schroner Z, Uličiansky V. Inhibítory SGLT2 – nová cesta v liečbe diabetes mellitus 2. typu. SchronerMED: Košice 2015. ISBN 978–80–8129–040–4.
26. Abdul-Ghani MA, Norton L, DeFronzo RA. Sodium-Glucose Cotransporter-2 Inhibitors and Type 2 Diabetes. In: Umpierrez GE. Therapy for Diabetes Mellitus and Related Disorders. 6th ed. American Diabetes Association: Virginia 2014 : 445–460. ISBN 978–1580405096.
27. Peters AL, Buschur EO, Buse JB et al. Euglycemic Diabetic Ketoacidosis: A Potential Complication of Treatment With Sodium–Glucose Cotransporter 2 Inhibition. Diabetes Care 2015; 38(9): 1687–1693.
28. Zinman B, Wanner Ch, Lachin JM et al. Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. N Engl J Med 2015. Dostupné z WWW:
29. Kohan DE, Fioretto P, Tang W et al. Long-term study of patients with type 2 diabetes and moderate renal impairment shows that dapagliflozin reduces weight and blood pressure but does not improve glycemic control. Kidney Int 2014; 85(4): 962–971.
30. Yale JF, Bakris G, Cariou B et al. Efficacy and safety of canagliflozin over 52 weeks in patients with type 2 diabetes mellitus and chronic kidney disease. Diabetes Obes Metab 2014; 16(10): 1016–1027.
31. Barnett A, Mithal A, Manassie J et al. Efficacy and safety of empagliflozin added to existing anatidiabetes treatment in patients with type 2 diabetes and chronic kidney disease: a randomized, double-blind, placebo–controlled trial. Lancet Diabetes Endocrinol 2014; 2(5): 369–384.
Štítky
Diabetologie Endokrinologie Interní lékařstvíČlánek vyšel v časopise
Forum Diabetologicum

2015 Číslo 3
-
Všechny články tohoto čísla
- Diabetes mellitus – osobitosti vo vyššom veku – klinický pohľad
- Pacient s diabetem z pohledu klinického nefrologa
- Včasný skríning a liečba spomaľujú progresiu diabetickej nefropatie
- Možnosti použitia inhibítorov DPP4 a SGLT2 u pacientov s diabetes mellitus 2. typu so zníženou funkciou obličiek
- Pohľad na kardiorenálny syndróm
- Najčastejšie infekčné komplikácie u diabetikov a ich liečba
- Rizikové faktory vzniku a progresie diabetickej retinopatie
- Obezita – kľúčový rizikový faktor pre diabetes mellitus po transplantácii obličky
- Obtížnost kontroly hypertenze u diabetické nefropatie
- Výskyt diabetickej nefropatie v populácii pacientov s diabetes mellitus na Slovensku: výsledky prieskumu NEFRITI
- Autodidaktický test hodnotený kreditmi SACCME
- Diabetológia na úsvite novoveku
- ESC Congress 2015: zamerané na redukciu kardiovaskulárneho rizika u diabetikov
- Stretnutie mladých diabetológov
- Forum diabetologicum 2015; 3
- Forum Diabetologicum
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Pohľad na kardiorenálny syndróm
- Najčastejšie infekčné komplikácie u diabetikov a ich liečba
- Výskyt diabetickej nefropatie v populácii pacientov s diabetes mellitus na Slovensku: výsledky prieskumu NEFRITI
- Včasný skríning a liečba spomaľujú progresiu diabetickej nefropatie
